|
|
综述:用于预测结直肠癌系统性治疗疗效的类器官和器官芯片研究进展发表时间:2023-03-02 18:19 结直肠癌(Colorectal cancer,CRC)是一组通常起源于异常隐窝病灶的异质性肿瘤疾病。结直肠癌的异质性可以表现出不同的临床和病理特征,从而导致不同的治疗结果和预后。因此,针对具有不同情况的不同患者,给与例如基因检测或循证医学等个性化治疗是必要的。仅依靠标准化诊断指南和分子测序不足以解决所有患者的问题。 人类癌细胞系是最常用的基础癌症和药物研究模型。然而,这些模型中很少有能够完全覆盖所有针对原发性肿瘤突变和转录异质性研究需求的。另一种体外模型是患者来源的异种移植物(PDX),这种模型具有更高的准确性,但构建难度相对较大。此外,其临床应用具有通量低和处理时间长的明显局限性。不过,由于异种移植物微环境的完整性,它目前仍然是验证肿瘤药物敏感性的金标准。 类器官是干细胞根据发育生物学原理自组织形成的三维细胞复合体,而器官芯片则是采用微芯片制造方法制造的微流控细胞培养装置。目前,癌症类器官和器官芯片适合作为临床转化和精准医疗的临床前模型(图1)。当下,类器官和器官芯片技术的重大进步促进了体外近生理三维组织和器官的构建。将可以精确复现肿瘤特征的类器官和器官芯片微环境整合,有望为加速临床转化提供巨大机会。 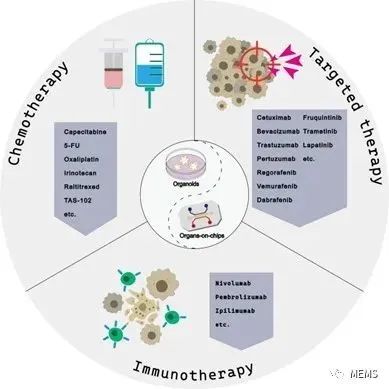 近期,南方医科大学以及南京金陵医院肿瘤内科的研究人员于Cell Death Discovery期刊发表了题为“Organoids and organs-on-chips: insights into predicting the efficacy of systemic treatment in colorectal cancer”的综述性论文。 该论文首先讨论了两种临床前模型——成人干细胞衍生的类器官系统和器官芯片技术在预测结直肠癌系统性治疗疗效方面的有效性。此外,该论文重点研究了基于这两种模型的体外和体内药物反应的一致性,以及基于这种预测有效性调整临床患者治疗策略以作为对临床治疗参考指标的补充的可行性。  最后,该论文讨论了这两种模型的局限性,并对类器官芯片技术的发展进行了展望。与癌细胞系相比,源自患者的类器官和器官芯片在培养过程中需要消耗更多的时间和资源。肿瘤类器官培养的主要限制包括微环境的缺乏、肿瘤细胞的短期扩增、来自正常类器官的污染、培养系统中血清和生长因子的影响,以及对小鼠来源的细胞外基质(ECM)的需求。与此同时,尽管模拟了一个相对完整的微环境,器官芯片还是受限于技术稳健性、时间成本、芯片原材料以及相对于类器官较低的3D结构复杂性。其中许多因素有可能影响对疗效的预测。例如,除了来自结直肠癌的类器官外,很多用于其他癌症药物疗效比较的类器官表现并不突出,这可能与微环境的缺乏直接相关。通常,有效的预测模型需要在有意义的短期临床治疗窗口中进行药物筛选。当然,对药物治疗的长期反应也很关键。在免疫治疗方面,长期的临床反应一直不尽如人意,这可以归因于与免疫微环境相关的免疫衰竭。因此,在模型的应用过程中,需要延长药物作用的持续时间,分析个体免疫细胞的内部变化并不断引入新的淋巴细胞或形成含有淋巴结的多器官器官芯片,以刺激免疫细胞在三级淋巴结构聚集。此外,存在少量潜在健康的类器官或特意引入健康的类器官可能会使药物反应的结果更加精确。这表明体外模型具有很大的改进潜力。 类器官芯片是类器官与器官芯片技术的结合。它本质上是干细胞领域和工程领域的协同。通过对类器官的进一步设计来控制干细胞行为和细胞微环境,可以打破类器官应用过程中的限制。器官芯片可以对靶器官进行人工构建及人为精确控制,而类器官可以遵循内在的发育程序进行自组装。这两种不同但互补的技术的融合已被大多数科学家接受。提高保真度和可重复性是类器官芯片的首要任务。此外,在类器官芯片的组装过程中,必须控制生物物理和生化微环境以及营养供应。  总体而言,虽然类器官芯片距离实用和广泛使用还有很长的路要走,但其在预测治疗疗效方面具有巨大的潜力。目前已有一定数量的基于这些模型的临床试验正在进行。在治疗时间窗、成本、药物筛选效率和准确性等方面,这些体外模型很可能在短期内就可以用作临床参考,并通过技术进步或技术融合指导个体患者治疗策略的优化。 论文链接: |

